Um cordão de monômeros de aminoácidos unidos por ligação peptídica forma uma proteína.
- existem 20 aminoácidos: 11 não-essenciais e 9 essenciais (que o corpo não produz)
- todos os 9 essenciais estão presentes no feijão, 8 em abundância 1, a metionina, está presente no arroz em abundância
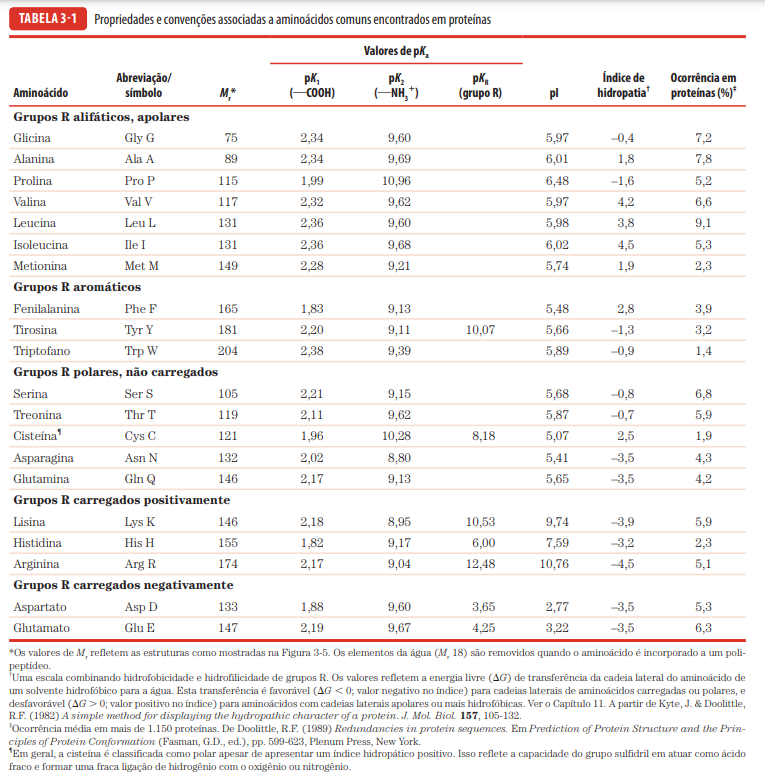
- todo aminoácido é composto por um carbono quiral ligado a uma carboxila (COOH ➙ desprotonamento ➙ COO–), um grupo amino (NH3+ ➙ desprotonamento ➙ NH2) e um hidrogênio (H) e, o que diferencia um aminoácido, outro grupo R (ionizável ou não)
- os aminoácidos são classificados pelo grupo R, definindo sua polaridade (apolar ou polar do grupo R), carga (neutro; positivo, que tem caráter básico; ou negativo, que tem caráter ácido) e pela estrutura do agrupamento (alifático, de cadeia aberta; alicíclico ou aromático)

- todos os aminoácidos forma enantiômeros, com ligações de forma idêntica porém invertida (espelhadas), L e D; essas diferenças na orientação espacial podem resultar em propriedades químicas e físicas diferentes.
- no corpo humano só temos aminoácidos L-
- proteínas: enzimas, hormônios, anticorpos transportadores, fibras musculares, cor dos olhos, unhas, cabelo, penas, teias de aranha, chifres de rinocerontes, antibióticos, venenos de cogumelos e uma miríade de outras substâncias com atividades biológicas
- participam de todos os processos biológicos
- depende da quantidade e do arranjo de aminoácidos
Ligação peptídica
Na formação da ligação peptídica, ocorre uma reação de condensação (união) entre o carbono do grupo carboxílico e o nitrogênio do grupo amino. Porém, para que isso aconteça, é necessário que ocorra uma desidratação, ou seja, a retirada de uma molécula de água.
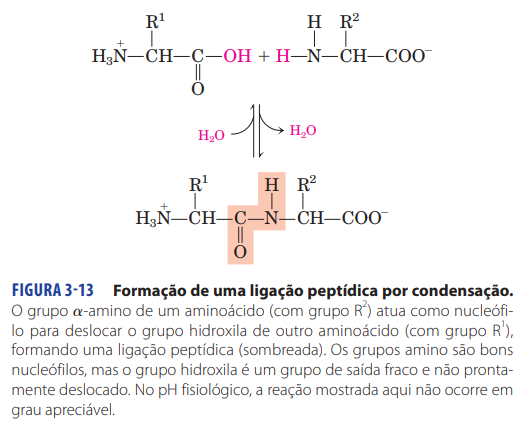
A desidratação que precede a ligação peptídica dá-se pela quebra da ligação entre o carbono e a hidroxila, na carboxila, e pela quebra de uma ligação entre o nitrogênio e um hidrogênio.
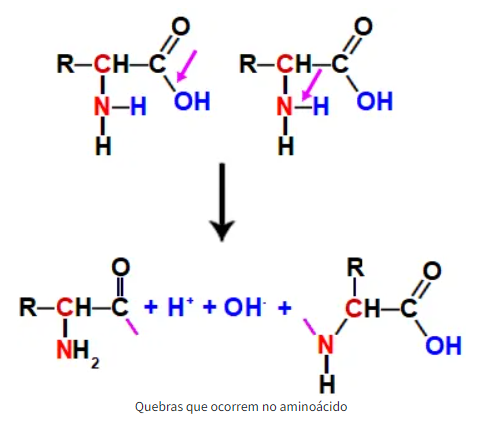
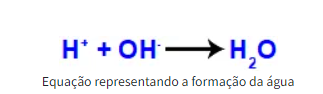
Com isso, ficam livres no meio reacional um hidrônio (H+) e um hidróxido (OH–), os quais, ao unirem-se, formam uma molécula de água.
Após a desidratação, haverá, no aminoácido, o carbono da carboxila com uma valência livre (ligação a ser feita) e o nitrogênio do grupo amino, também com uma valência livre.
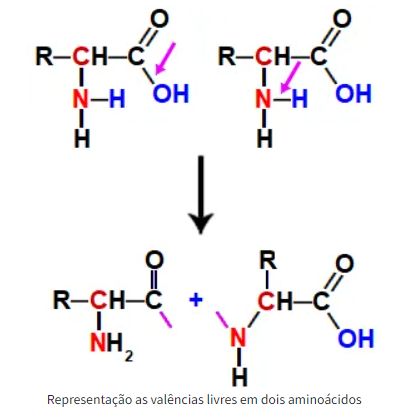
A ligação peptídica ocorre exatamente quando a valência livre no carbono de um aminoácido encontra a valência livre no nitrogênio de outro aminoácido, resultando em uma única ligação covalente entre eles.
Na imagem abaixo, o destaque em laranja mostra 4 ligações peptídicas, unindo 5 aminoácidos.

A ligação peptídica ocorre no ribossomo, durante a tradução do RNA na síntese de proteína. Demanda alta energia de ativação.
Saiba mais:
Aula USP: Aminoácidos, peptídeos e proteínas – Parte 1
Aula USP: Aminoácidos, peptídeos e proteínas – Parte 2