Aula 24/10 | professor Paulo Sergio Taube (pstjunior@yahoo.com.br)
Ligação iônica – eletrostática, muito forte
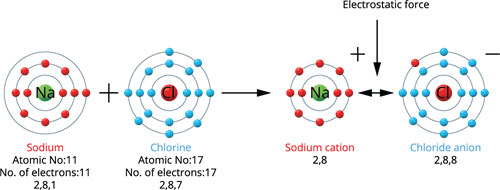
Um íon dá e outro íon recebe o elétron na camada de valência, em busca de estabilidade:
- a ligação iônica é resultado de uma interação eletrostática entre íons de cargas opostas (cátions e ânions);
- os íons reagem entre si a fim de alcançarem a estabilidade;
- é uma interação geralmente estabelecida entre um metal e um ametal (não metal);
- os compostos iônicos, geralmente:
- são duros e quebradiços;
- têm alto pontos de fusão e ebulição;
- conduzem corrente elétrica quando dissolvidos em água.
Na++Cl– = NaCl (Cloreto de sódio ou sal de cozinha)
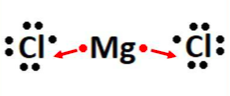
Mg+2+Cl– = MgCl2 (Cloreto de Magnésio)
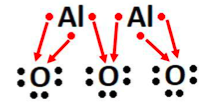
Al3+O2- = Al2O3 (Óxido de Alumínio)
Ligação covalente
- a ligação covalente é resultado de um compartilhamento de elétrons, geralmente estabelecida entre um ametal e um ametal;
- os compostos covalentes são:
- muito mais comum no planeta, principalmente por causa do carbono, que é da família 4A e tem 4 elétrons na camada de valência, podendo fazer 4 ligações
Compartilhamento de elétrons:
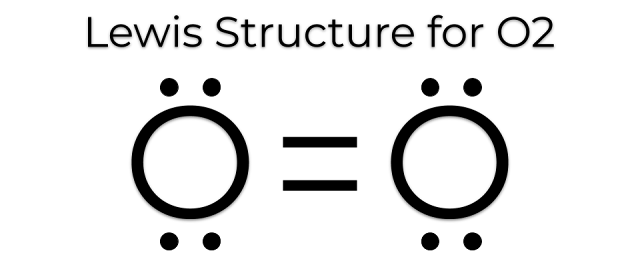
Apolar: entre átomos iguais (O2; H2; N3)
Ligação Sigma (σ) e Pi (π)
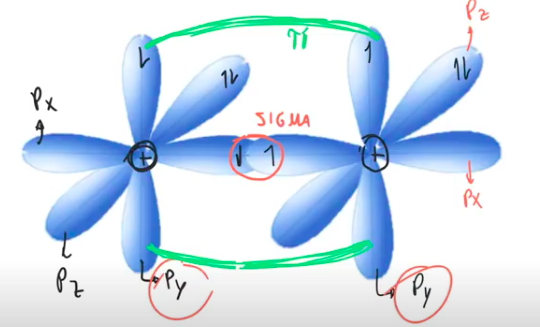
Quando há mais de uma ligação, uma é sigma e a(s) outra(s) é(são) Pi:
- a sigma é uma ligação frontal nos orbitais (em vermelho na imagem abaixo), entre o núcleo dos dois átomos, sendo mais forte;
- a Pi é uma ligação paralela nos orbitais (em verde na imagem abaixo), longe do núcleo, sendo mais fraca.
Ligação coordenada, antigamente chamada de dativa
Outro exemplo, CO, sendo que o C faz duas covalentes e uma coordenada simples
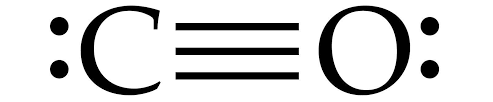
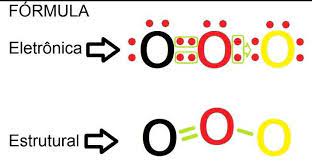
Outro exemplo de coordenada
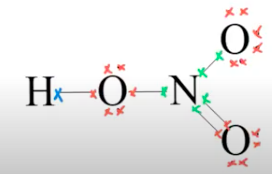
Exceções à regra do Octeto (gases nobres) e Dueto (H e He)
Alguns compostos não precisam ter oito elétrons na camada de valência para atingir a estabilidade, são por isso considerados exceções à Regra do Octeto.
Átomos do período 2 (com até duas camadas) que são muito pequenos e por isso tem uma eletrosfera muito grudada no núcleo, sendo muito difícil pegar elétrons deles.
BeH2 , Hidreto de berílio
O Berílio (Be) é da família 2A e do 2º período. Ele tem 2 elétrons na camada de valência e tem duas camadas K e L, mas é um átomo muito pequeno, com massa muito pequena e a eletrosfera muito colada no núcleo. É díficil arrancar elétrons dele. Na ligação com o Hidrogênio (H), ele faz 2 co-valentes e fica estável com 4é, sendo uma exceção à regra de octeto.
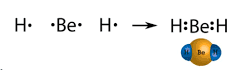
Por que o hidreto de berílio é um composto covalente e não iônico? Os hidretos dos outros elementos do período 2 (Sr. Becamgbara) são iônicos, ou seja, consistem em sólidos formados por um cátion M 2+ e dois ânions H – hidreto (MgH 2 , CaH 2 , BaH 2 ). Portanto, BeH 2 não consiste em Be 2+ ou H – interagindo eletrostaticamente. O cátion Be 2+ é caracterizado por seu alto poder de polarização, que distorce as nuvens eletrônicas dos átomos circundantes.
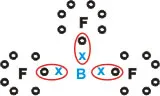
BF3 , Trifluoreto de boro
O Boro (B) é da família 3A e do 2º período. Ele tem 3 elétrons na camada de valência e tem duas camadas K e L, mas é um átomo muito pequeno, com massa muito pequena e a eletrosfera muito colada no núcleo. É díficil arrancar elétrons dele. Na ligação com o Flúor (F), ele faz 3 co-valentes e fica estável com 6é, sendo uma exceção à regra de octeto.
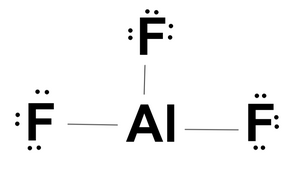
AlF3 , Fluoreto de Alumínio
O Alumínio atinge a estabilidade com seis elétrons na camada de valência. O átomo de Alumínio tende a doar seus elétrons e assim pode formar três ligações simples com outros átomos.
Hibridização, ressonância e orbitais sp3
pp
Geometria molecular
pp
Ligação metálica
Principais ligas metálicas
- ouro 18 quilates (Au e Cu)
- aço (Fe e C)
- bronze (Cu e Zn)
- metal monel (Ni e Cu)
- amálgama de prata (Hg e Ag)
- liga leve (Mg e Al)
- solda (Pb e Sn)
Ligação polar e apolar
Na geometria molecular:
- se a resultante for nula, a molécula é apolar
- se a resultante for não nula, a molécula é polar.
- se a ligação for do mesmo elemento, é apolar.
Ligação entre moléculas – intermolecular
Ponte de Hidrogênio, ligação super-forte entre moléculas
Atrações entre moléculas que contêm H ligado diretamente a um desses três elementos mais eletronegativos F, O, N.
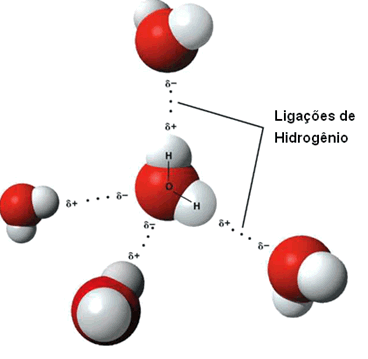
Lembrando os elementos mais eletronegativos, do maior F para o menor H
F ➞ O ➞ N ➞ Cl ➞ Br ➞ I ➞ S ➞ C ➞ P ➞ H
Dipolo-Dipolo, ligação moderada entre moléculas, mas alto ponto de ebulição
Atrações entre duas moléculas polares, que semelhante a uma pilha apresenta dois pólos – negativo e positivo.

.
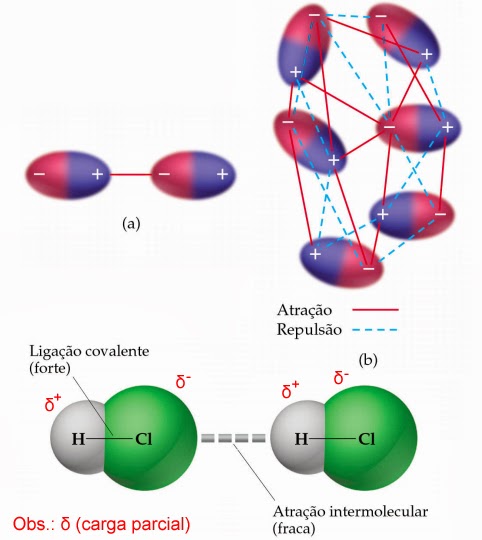
Na molécula de HCl (gás clorídrico) a nuvem eletrônica está mais deslocada no sentido do átomo de cloro, pois ele é mais eletronegativo que o hidrogênio.
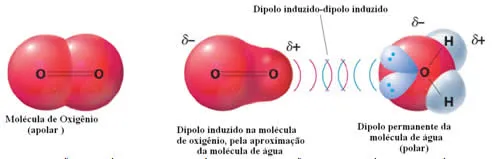
Dipolo instantâneo gerando dipolo induzido, ligação fraca entre moléculas
As forças dipolo instantâneo-dipolo induzido ocorrem por uma deformação momentânea na nuvem eletrônica da molécula entre moléculas apolares, entre átomos de gases nobres ou entre moléculas polares e apolares. Desse modo, os elétrons se acumulam em determinado lado, que fica polarizado negativamente e o lado oposto positivamente, em razão da deficiência de carga negativa.
Aula resumo
Moléculas diatômicas e poliatômicas
Solubilidade
- solvente-solvente
- soluto-soluto
- solvente-soluto
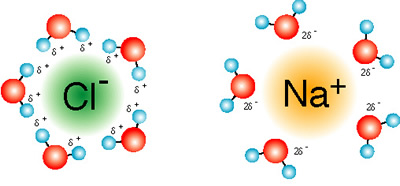
Íon-Dipolo
Como o solvente se comporta com ele mesmo. Soluto iônico interage com a água é o íon-dipolo.
exemplo: água H2O + sal NaCl, solúvel em água
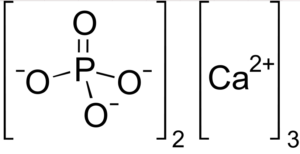
exemplo: água H2O + fosfoto de cálcio Ca3PO4, não solúvel em água
Tem duas interações, sendo muito pouco solúveis em água.
Álcool e ácidos de cadeias longas
Pouco solúvel em água
Álcool e ácido de cadeia curta
Mais solúvel em água